臨床成績
「禁忌を含む注意事項等情報」等は電子添文をご参照ください。

左室駆出率≧40%の慢性心不全患者※を対象に心血管複合エンドポイントを主要評価項目とした国際共同第Ⅲ相試験
※:本剤の効能又は効果(抜粋):「慢性心不全 ただし、慢性心不全の標準的な治療を受けている患者に限る。」
承認時評価資料(Solomon SD, et al. N Engl J Med. 2024; 391(16): 1475-1485.)
[COI]本試験はバイエルの資金により行われた。また、著者にバイエルの社員及びバイエルよりコンサルト料等を受領している者が含まれる。
有効性
主要評価項目(検証的解析結果):心血管複合エンドポイント※1
ケレンディア群は心血管複合エンドポイント※1の発現リスクを16%有意に低下させました[検証的解析結果、p=0.007、層別Andersen-Gillモデル(層別因子:地域及びLVEF)]
心血管複合エンドポイント(心血管死及びすべての心不全イベント)※1
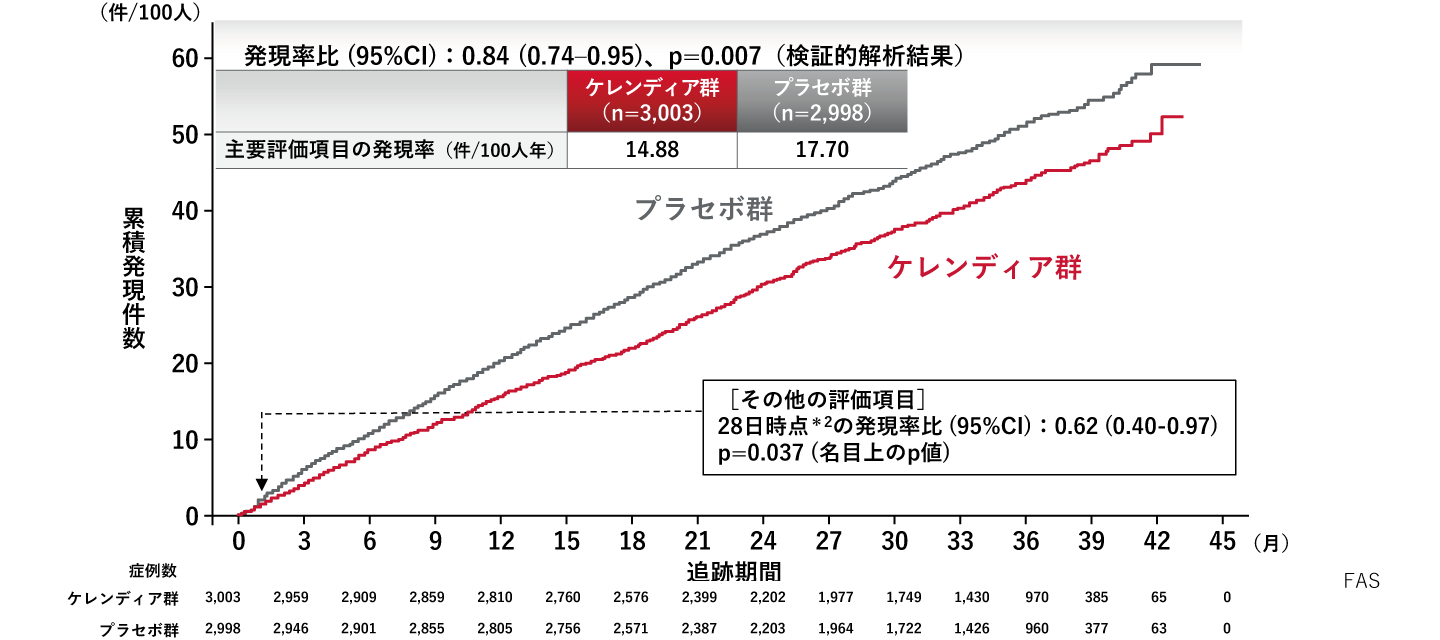
解析方法:層別Andersen-Gillモデル(層別因子:地域及びLVEF)、有意水準:0.04967
FAS
※1:心血管死及びすべての心不全イベント(初発及び再発を含む心不全による入院または緊急受診)
心血管複合エンドポイント※1[主要評価項目、(検証的解析結果)]
及び構成要素[副次評価項目及びその他の評価項目]
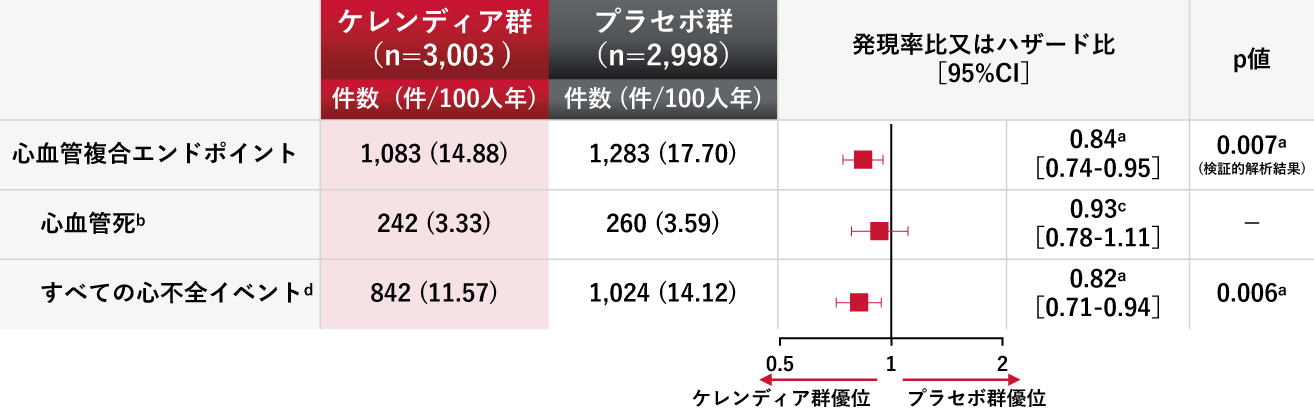
FAS
a:解析方法:層別Andersen-Gillモデルによる発現率比及びp値(層別因子:地域及びLVEF)、有意水準:0.04967
b:その他の評価項目
c:解析方法:層別Cox比例ハザードモデルによるハザード比(層別因子:地域及びLVEF)
d:副次評価項目:すべての心不全イベント(初発及び再発を含む心不全による入院または緊急受診)
※1:心血管死及びすべての心不全イベント(初発及び再発を含む心不全による入院または緊急受診)
主要評価項目のサブグループ解析:患者背景別の心血管複合エンドポイント※1
いずれのサブグループにおいても発現率比は1を下回りました(探索的結果)
患者背景別の心血管複合エンドポイント※1
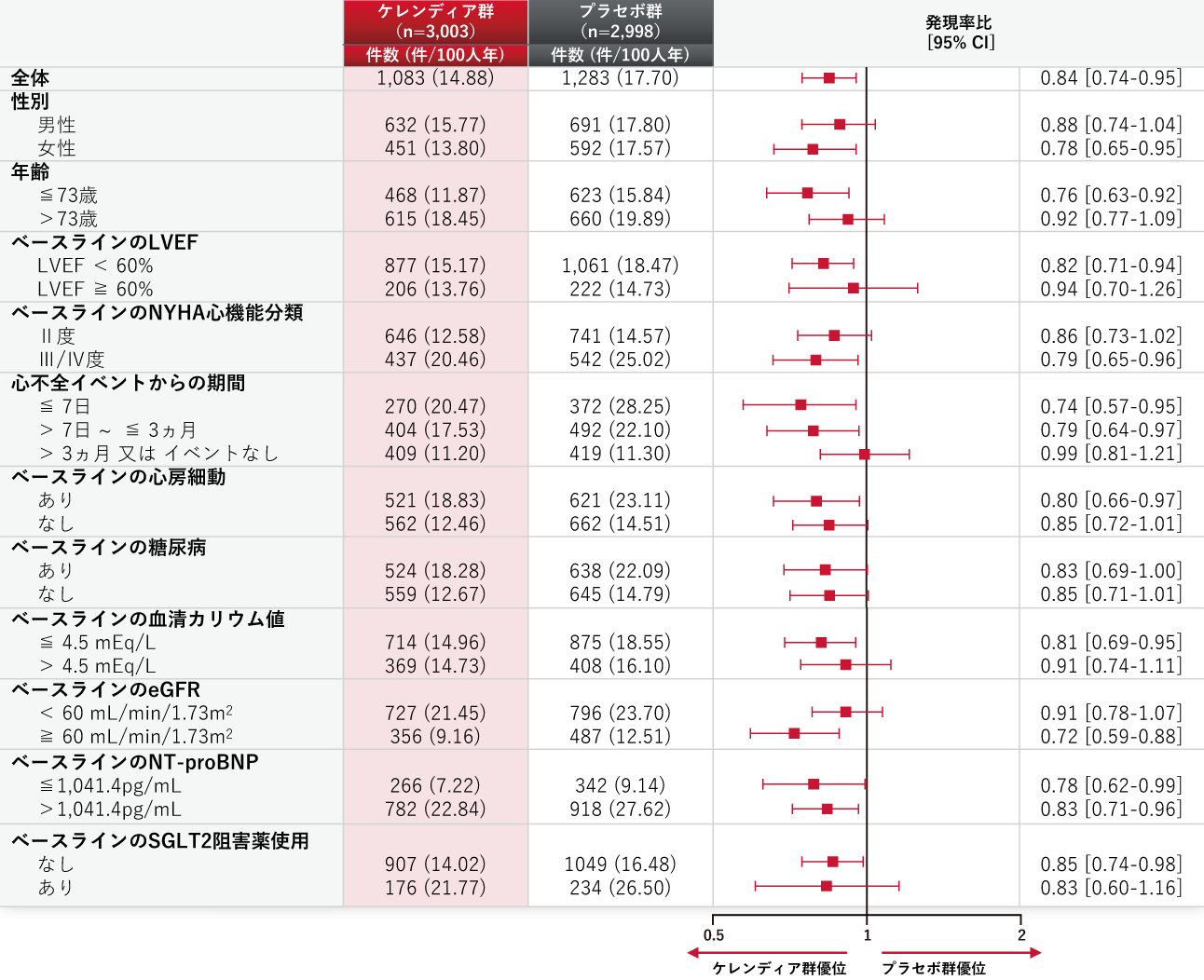
FAS
解析方法:層別Andersen-Gillモデル(層別因子:地域及びLVEF)
※1:心血管死及びすべての心不全イベント(初発及び再発を含む心不全による入院または緊急受診)
安全性
安全性評価項目:副作用
副作用は、ケレンディア群19.2%、プラセボ群10.8%に認められました
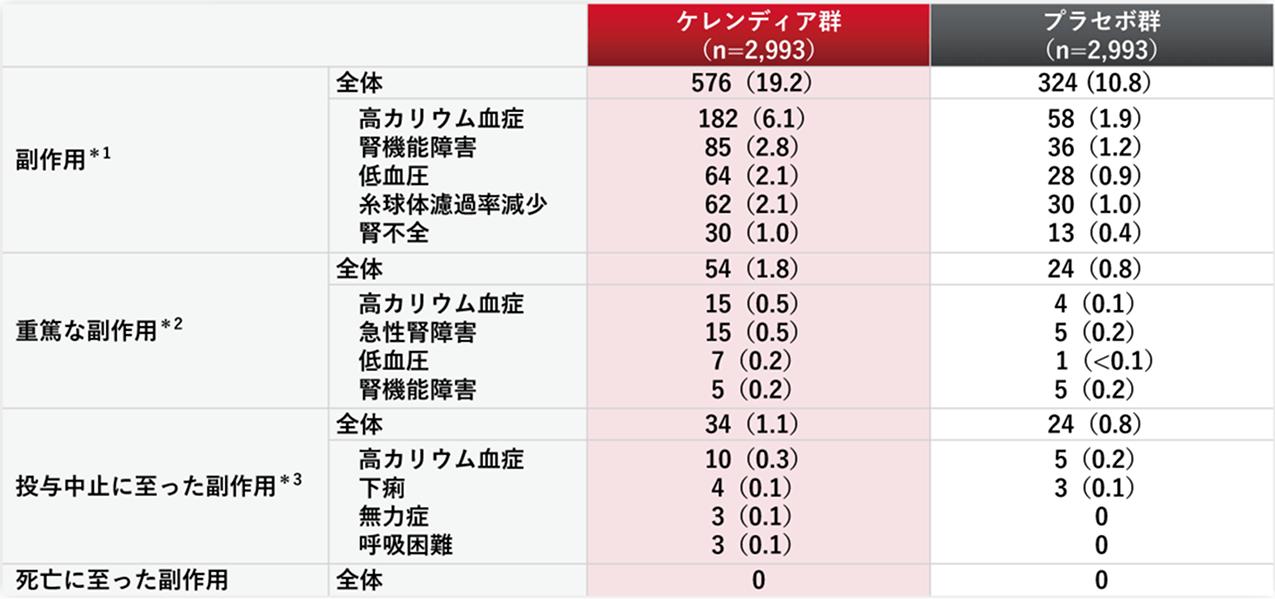
SAF
MedDRA version:27.0
発現例数(%)
*1:ケレンディア群で1%以上発現した副作用
*2:ケレンディア群で0.2%以上発現した副作用
*3:ケレンディア群で0.1%以上発現した副作用
医薬品リスク管理計画において、高カリウム血症は重要な特定されたリスク及び安全性検討事項に設定されているため紹介しています
安全性評価項目:血清カリウム値
ケレンディア投与開始1ヵ月後より、血清カリウム値の上昇がみられました
血清カリウム値の経時的変化
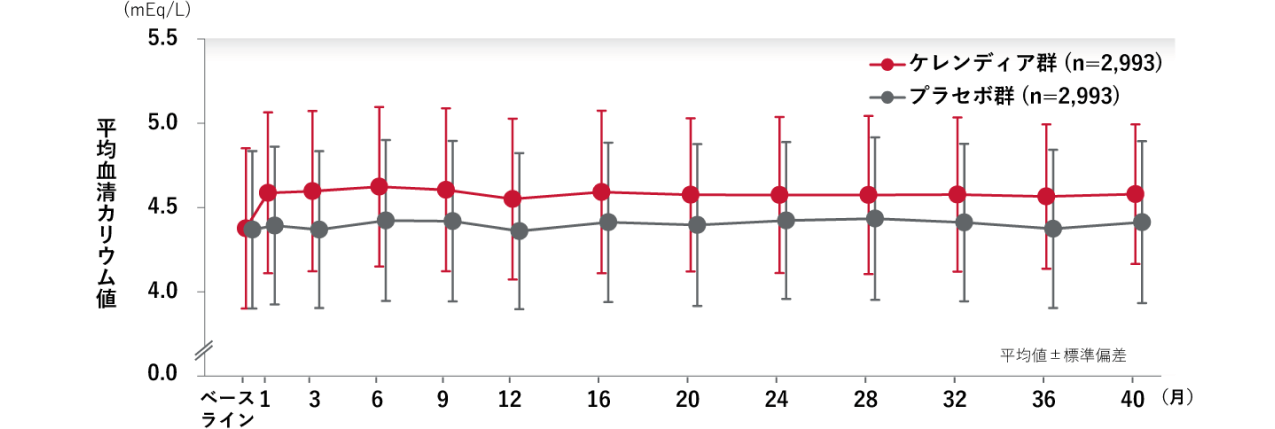
SAF
患者背景
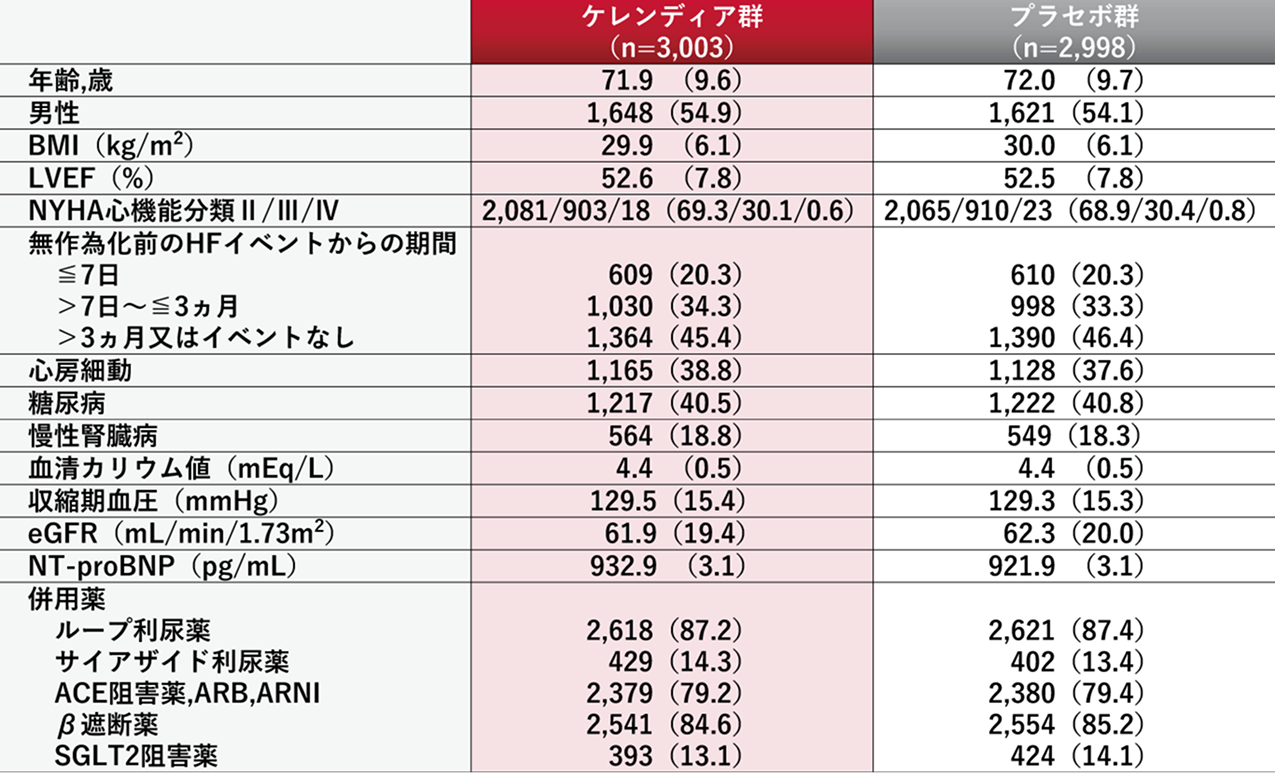
FAS
平均値(標準偏差)またはn(%) NT-proBNPのみ幾何平均値(幾何標準偏差)












